Elektrokimia

Elektrokimia uyito-yito tango ilimu kimia fisik u mopo'otuota bibilohu kelistrikan mondo reaksi kimia. Elemen u popohuna modelomo reaksi elektrokimia dikarakterisasikan wolo dadaata liyo elektron u dimiliki. Lo'u uumumu elektrokimia terbagi modelomo duluwo kolompok, de'uyito-yito sel gavani wau sel elektrolisis.[1] Reaksi elektrokimia mowali pilopona'olio wolo spontan, de'uyito-yito to'u duluwo elektroda u wahuma to delomo cairan elektrolit popoaito lo lililo listrik.[2] Elektrokimia popohuna ode pemurnian wau pelapisan logam wawu elektrosintesis.[3]
Jenis
[boli'a | boli'a bungo]Metode elektrokimia didasarkan to reaksi redoks u mopogabungi proses oksidasi wau reduksi. Reaksi botia pohutuo to elektroda u sama mealo u hihide. Sistem elektrokimia motitihutu melalui reaksi elektrokimia u sababuo ole sel elektrokimia. Sel elektrokimia terbagi mowali duluwo jenis de'uyito-yito sel galvani wau sel elektrolisis. Sel gavani mo'otapu listrik sababu woluo olio reaksi spontan, hiambola sel elektrolisis mo'otapu listrik sababu woluo olio reaksi u diila spontan.[3]
Redoks
[boli'a | boli'a bungo]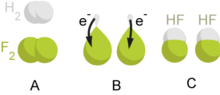
Redoks mowali istilah u mopopatata moboli'a olio bilangan oksidasi (keadaan oksidasi) atom-atom modelomo ngobotu reaksi kimia. Istilah redoks londo duluwo konsep, de'uyito-yito reduksi wau oksidasi.[4][5]
Oksidator dan reduktor
[boli'a | boli'a bungo]Oksidator uyito-yito zat u mengoksidasi zat uwewo modelomo tuwawu reaksi redoks. Hiambola reduktor uyito-yiro zat u mereduksi zat uwewo modelomo tuwawu reaksi redoks.[6]
- Oksidator uwito zat yang mengalami reduksi.
- Reduktor uwito zat yang mengalami oksidasi.
Fenomena alam
[boli'a | boli'a bungo]Korosi
[boli'a | boli'a bungo]Korosi mowali rusa logam u yiloali akibati reaksi elektrokimia ataupun reaksi kimia wolo turusi. Poristiwa korosi u uumumu da'a lotapu uyito-yito karat to wuate, noda pada perak, wawu platina moyidu u motitihutu to tembaga wau kuningan. Medium korosi mowali to keadaan mohengu mealo mobata. Contoh korosi u pilopona'o olio to delomo medium kohengu de'uyito-yito karat logam wuate ole gas oksiden mealo ole gas belerang dioksida. Hiambola contoh korosi u pilopona'olio modelomo medium mobata de'uyito-yito wuate waun wahuma to molotingo klorida. Rusa lo akiibati korosi mongohi u'ilorugia to bidang industri mealo ekonomi.[7]
Penerapan
[boli'a | boli'a bungo]Elektrosintesis
[boli'a | boli'a bungo]Elektrosintesis uwito tilala tuawu teknik sintesis u popopasio to bahan anorganik. Prinsip duduta'a elektrosintesis uyito-yito elektrokimia. Peralatan u popohuna to proses elektrosintesis de'uyito-yito duluwo mealo tolo batango elektroda u popoaito lo tolohu listrik. Pengaturan linggahu rekasi pohutuo lo'u mongaaturu hihede potensial wau lenggota kerapatan tolohu listrik to batas-batas u diinginkan. Sintesis u mopohuna metode elektrosintesis gaambangi ma'o kawasa wau o lenggota polusi u mopa da'a.[3]
Referensi
[boli'a | boli'a bungo]- ↑ Harahap, Muhammad Ridwan (2016-07-01). "Sel Elektrokimia: Karakteristik dan Aplikasi". CIRCUIT: Jurnal Ilmiah Pendidikan Teknik Elektro (dalam bahasa Indonesia). 2 (1). doi:10.22373/crc.v2i1.764. ISSN 2549-3701.
- ↑ "Electrochemical reaction | chemistry". Encyclopedia Britannica (dalam bahasa Inggris). Diakses tanggal 2021-04-30.
- ↑ Lompat ke: 3,0 3,1 3,2 Ningsih, Sherly Kasuma Warda (2016). Sintesis Anorganik (PDF). Padang: UNP Press. ISBN 978-602-1178-14-0.
- ↑ "Redox Reactions". www.chemistry.wustl.edu. Diakses tanggal 2021-04-30.
- ↑ "Definitions of oxidation and reduction (redox)". www.chemguide.co.uk. Diakses tanggal 2021-04-30.
- ↑ "Oxidizing and Reducing Agents". chemed.chem.purdue.edu. Diakses tanggal 2021-04-30.
- ↑ Subarkah, C. Z., dan Chusni, M. M. (2018). Nilai Keislaman pada Pembelajaran Elektrokimia Diarsipkan 2021-08-31 di Wayback Machine. (PDF). Bandung: Pusat Penelitian dan Penerbitan, Universitas Islam Negeri Sunan Gunung Djati Bandung. hlm. 69. ISBN 978-602-582-301-5.
